¿Cómo trataremos la metástasis en un futuro?
Una revisión sobre las estrategias emergentes para el tratamiento de la metástasis.
Bienvenido a una nueva entrega de nuestro blog!
Por si no me conoces me presento, me llamo Daniel Lucena y soy especialista en ejercicio y cáncer.
En este blog, comparto cada semana mis aprendizajes sobre todo lo relacionado con el cáncer y cómo el ejercicio físico actúa contra él.
Hoy en concreto, voy a explicarte este artículo: Emerging strategies for treating metastasis
En español sería algo así como: “Estrategias emergentes para el tratamiento de la metástasis”.
Espero que lo disfrutes!
La diseminación sistémica de células tumorales es la principal causa de la mayoría de las muertes por cáncer. Sin embargo, han surgido pocas estrategias terapéuticas efectivas que se enfoquen específicamente en la metástasis. En esta nueva entrega, analizo los avances recientes en la comprensión de las vías intrínsecas del tumor que impulsan la colonización metastásica y la resistencia a los tratamientos, así como las estrategias de activación inmunitaria para combatir la enfermedad metastásica.
Voy a centrarme en mecanismos terapéuticamente aprovechables, estrategias prometedoras en desarrollo preclínico y clínico, y áreas emergentes con el potencial de convertirse en tratamientos innovadores.
¿Preparado? Vamos allá.
La mayoría de los fármacos aprobados para el tratamiento del cáncer, incluidos los inhibidores de la tirosina quinasa (TKI), las terapias citotóxicas sistémicas (quimioterapia) y los conjugados anticuerpo-fármaco (ADC), no logran un impacto duradero en casos de enfermedad metastásica avanzada, a menudo debido a la aparición de mecanismos de resistencia terapéutica adquirida. Por otro lado, la posibilidad de remisiones duraderas tras el tratamiento con inmunoterapias ha marcado un cambio de paradigma para los pacientes con cáncer en estadio IV, quienes antes recibían diagnósticos terminales.
Estos avances en inmunoterapia han dado lugar a una nueva era en la que los pacientes con cáncer avanzado pueden aspirar a una remisión prolongada o al manejo crónico de las metástasis.
Por qué la metástasis debe ser una consideración principal en el desarrollo de fármacos oncológicos.
Es difícil cuantificar la cifra de muertes causadas por el cáncer metastásico, ya que la enfermedad se manifiesta en múltiples órganos y la forma de reportar la mortalidad varía entre los sistemas de salud y los distintos tipos de cáncer.
Se observan cargas de mortalidad comparables debidas a la metástasis en todos los tipos de tumores sólidos, lo que subraya la necesidad de implementar enfoques preventivos y terapéuticos para reducir el impacto del cáncer metastásico y lograr un cambio significativo en las tasas de mortalidad por cáncer.
Han surgido dos modelos generalizados de progresión metastásica:
Cánceres que metastatizan en función del tiempo y/o el tamaño del tumor.
Aquellos que metastatizan debido a la célula de origen específica y/o a la línea mutacional.
Modelo 1: Este modelo sugiere que la metástasis ocurre como resultado de la evolución natural del tumor. A medida que pasa el tiempo o el tumor crece y alcanza cierto tamaño, aumenta la probabilidad de que las células cancerosas se desprendan y se diseminen a otras partes del cuerpo. En este caso, la metástasis depende más de la duración del tumor en el organismo o de su tamaño crítico.
Modelo 2: Este modelo se enfoca en las características biológicas intrínsecas de las células cancerosas. Aquí, la capacidad de metastatizar depende de la célula original de donde se originó el tumor o de las mutaciones específicas que han ocurrido durante su desarrollo. Algunos tipos de cáncer tienen mayor propensión a la metástasis debido a su tipo celular o a las alteraciones genéticas que promueven la capacidad de las células cancerosas para invadir otros tejidos.
Cánceres comunes como los de mama, colon, riñón, pulmón y próstata pertenecen al grupo de los que metastatizan temprano. Aunque algunos casos nunca llegan a diseminarse, entre un 10% y 15% de los cánceres de mama desarrollan metástasis en un plazo de 3 años. Además, la caracterización genética ha revelado la existencia de tumores primarios que comienzan a diseminarse desde etapas muy tempranas.
Por lo tanto, aunque la detección y diagnóstico temprano pueden ayudar a mejorar la supervivencia en algunos tipos de cáncer, siempre será necesario contar con terapias efectivas que se enfoquen en la enfermedad metastásica dentro del arsenal médico.
Limitaciones de las terapias dirigidas
El informe del Programa de Vigilancia, Epidemiología y Resultados Finales (SEER) del Instituto Nacional del Cáncer (NCI) de 2020 destacó que parte de la reducción en la mortalidad por cáncer se puede atribuir a avances clave en terapias dirigidas e inmunoterapias, que son muy efectivas en el tratamiento del melanoma metastásico y los cánceres de pulmón.
En cambio, la mayoría de los más de 200 fármacos aprobados para tratar el cáncer han tenido poco impacto en la reducción de la mortalidad, lo que revela una desconexión evidente entre la aprobación de los medicamentos y los beneficios para los pacientes. Las mejoras en el tratamiento del cáncer, que incluyen cirugía, radioterapia, quimioterapia y terapias dirigidas, contribuyeron entre un 4% y un 8% a la disminución de la mortalidad por cáncer entre 1991 y 2011.
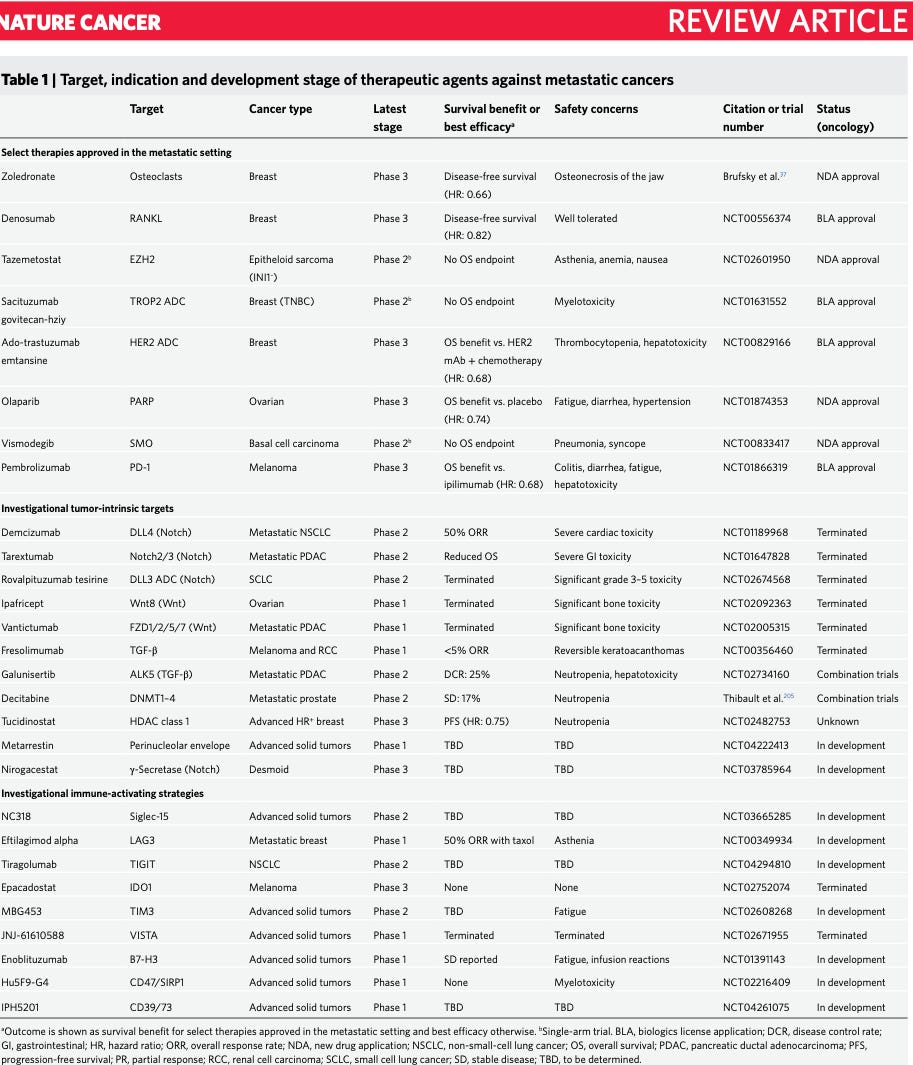
Tabla 1: Objetivo, indicación y etapa de desarrollo de agentes terapéuticos contra cánceres metastásicos
Gran parte de la reducción de la mortalidad atribuida a los tratamientos se debe a los avances en la terapia adyuvante (quimio, radio, hormonoterapia…) que previene la recaída metastásica al eliminar las células tumorales diseminadas.
Varios tratamientos convencionales han demostrado su capacidad para prolongar la supervivencia en el contexto adyuvante, como el trastuzumab (anti-HER2) y la quimioterapia en el cáncer de mama, apalutamida en el cáncer de próstata, quimioterapia en los cánceres de pulmón y colon, e imatinib en los tumores gastrointestinales.
Aunque la terapia adyuvante para prevenir la recaída es hoy en día la estrategia más efectiva para reducir la mortalidad por cáncer después del diagnóstico, su aprobación en este contexto requiere ensayos clínicos con un gran poder estadístico y de larga duración, lo que muchas veces no es viable para estudios que buscan una primera aprobación.
Además, identificar subgrupos responsivos y la farmacodinámica predictiva añade complejidad a estos desafíos. Por ejemplo, el tratamiento adyuvante con inhibidores de la resorción específicos para metástasis ósea solo es efectivo en el subgrupo de pacientes con cáncer de mama postmenopáusicas.
Y siempre hay que tener en cuenta los toxicidades que genera un fármaco.
El tratamiento adyuvante a largo plazo puede verse limitado por toxicidades crónicas, como la cardiotoxicidad asociada con el trastuzumab. Por lo tanto, el marco regulatorio y financiero actual para el desarrollo de fármacos contra el cáncer no es que facilite la creación de terapias específicas para la metástasis (y no tiene por qué hacerlo).
Una Curiosidad:
Los intentos de orientar terapias específicas hacia las vías metastásicas han fracasado casi de manera universal. En la vanguardia de este esfuerzo se encuentran numerosos ensayos que buscan inhibir las metaloproteinasas de matriz (MMPs). Modelos experimentales sugirieron que las MMPs eran fundamentales en la metástasis del cáncer al aumentar la motilidad celular y la invasión (la motilidad es un término de la biología para expresar la habilidad de moverse espontánea e independientemente).
Sin embargo, los ensayos clínicos de inhibidores de MMP mostraron una falta de respuesta o peores resultados. Aunque el fracaso se ha atribuido a una comprensión incompleta de la especificidad de las MMPs, a protocolos inadecuados en los ensayos clínicos y a efectos no intencionados sobre el sistema inmunológico, la razón fundamental probablemente radica en que las terapias dirigidas a la invasión, migración y extravasación pueden no ser efectivas para tratar enfermedades metastásicas establecidas. Una gran cantidad de evidencia muestra que los cánceres liberan de manera no específica células competentes para metástasis, y los pacientes pueden albergar células cancerosas dormidas competentes para metástasis antes del diagnóstico y tratamiento.
La conexión entre Capacidad Metastásica, Resistencia Terapéutica y Plasticidad ofrecen Nodos Terapéuticos prometedores.
La capacidad metastásica, la resistencia terapéutica y la plasticidad están intrínsecamente relacionadas a través de vías genéticas, epigenéticas y metabólicas que ofrecen nodos terapéuticos prometedores para el desarrollo de fármacos.
Para explicarte esto, voy a utilizar una metáfora.
Vamos a imaginarnos que el cáncer es como un árbol que crece en un jardín. Este árbol no solo se queda en un lugar; sus raíces pueden extenderse a otras partes del jardín. Esta capacidad de extenderse se llama "capacidad metastásica". Además, el árbol también puede volverse fuerte contra los intentos de talarlo, lo que se conoce como "resistencia terapéutica".
Para entender cómo crece y se fortalece este árbol, necesitamos ver lo que sucede por debajo del suelo. Este suelo está compuesto de muchas cosas: elementos genéticos (como las semillas), epigenéticos (que son como fertilizantes que pueden cambiar la manera en la que crece el árbol) y metabólicos (que son como los nutrientes que alimentan al árbol). Estos elementos están todos conectados y ofrecen puntos donde los jardineros (los científicos) pueden intervenir y ayudar a controlar el crecimiento del árbol.
Por ejemplo, hay "fertilizantes" especiales (modificaciones epigenéticas) que pueden ayudar al árbol a crecer más rápido y volverse más resistente. Pero, aunque estos fertilizantes ayudan, también pueden hacer que el árbol se vuelva más complicado de manejar, ya que puede cambiar de forma (plasticidad) y adaptarse a diferentes condiciones del jardín.
La capacidad del árbol para crecer y adaptarse también está relacionada con cómo utiliza sus recursos (metabolismo). Si el árbol encuentra maneras eficientes de absorber agua y nutrientes (como los caminos que generan NAD(P)h), se vuelve aún más fuerte. NAD(P)H es una coenzima que juega un papel crucial en el metabolismo celular.
Los jardineros quieren encontrar formas de detener el crecimiento del árbol, pero no es fácil. A veces, los tratamientos (como la cirugía o la quimioterapia) funcionan, pero a menudo el árbol encuentra la manera de sobrevivir y seguir creciendo. Por eso, los científicos están buscando nuevas estrategias para atacar las raíces y las ramas del árbol que son responsables de su capacidad para crecer y adaptarse, buscando un enfoque que funcione ya sea solo o en combinación con tratamientos más tradicionales.
Y las nuevas posibles estrategias son…
Se han validado algunos objetivos candidatos como nodos clave de regulación que son comunes a diferentes tipos de cáncer.
Enfoque en la plasticidad fenotípica y la resistencia al estrés
El concepto de desdiferenciación y plasticidad fenotípica ha sido fundamental en la investigación sobre la metástasis, ya que los cánceres menos diferenciados presentan un mayor riesgo de metástasis y resistencia a tratamientos.
Un cáncer poco diferenciado se refiere a un tipo de cáncer en el cual las células tumorales tienen un aspecto y comportamiento menos similar a las células normales del tejido del que se originan.
Este concepto ha evolucionado con el tiempo, abarcando procesos como la transición epitelio-mesenquimal (EMT), la transición mesenquimal-epitelial (MET) y la hipótesis de las células madre cancerosas (CSC). A pesar de las controversias sobre la importancia de la EMT y las CSC en diferentes tipos de cáncer, se ha demostrado que las transiciones celulares hacia estados similares a células madre son clave para la resistencia a tratamientos.
En los últimos años, se ha vinculado la plasticidad celular con la metástasis, mientras que se ha reconocido que los cambios en el estado celular son fundamentales para la resistencia terapéutica.
La plasticidad celular se refiere a la capacidad de las células para cambiar y adaptarse. Se ha descubierto que esta capacidad está relacionada con la metástasis. Además, estos cambios en las células también son importantes para que los tratamientos contra el cáncer sean menos efectivos.
Hay genes, como el MTDH, que son clave en este proceso. Estos genes ayudan a que las células mantengan características de células madre, lo que les permite ser más flexibles y resistentes. También están involucrados en la transición de las células de un tipo a otro, lo que puede facilitar la metástasis y la resistencia al estrés.
Por lo tanto, enfocar las estrategias terapéuticas en los reguladores de la plasticidad se ha convertido en una estrategia crítica para combatir el cáncer metastásico.
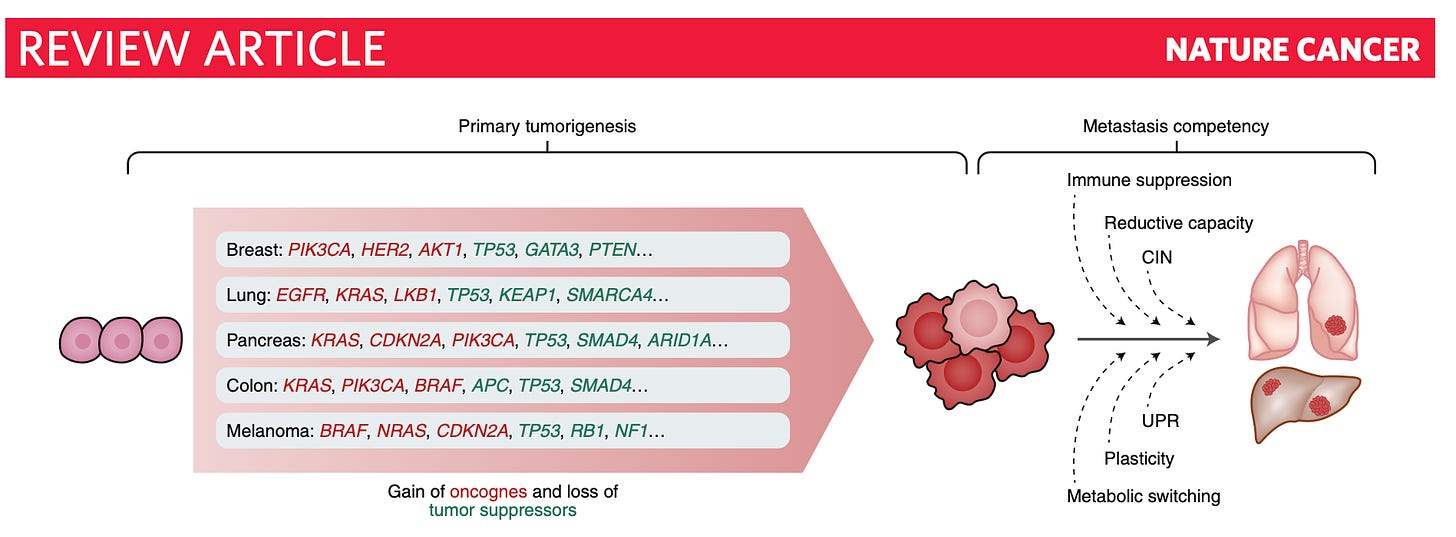
Desarrollar la capacidad para diseminarse (metástasis) requiere que las células cancerosas tengan más características malignas además de las que ya tienen en el tumor original. Los diferentes tipos de tumores primarios cambian de manera gradual, y cada vez que ocurre una nueva mutación en un gen que controla el crecimiento celular (ya sea un supresor tumoral o un oncogén), el tumor gana una pequeña ventaja competitiva.
Las mutaciones que causan cáncer suelen ser diferentes según el tipo de cáncer, y se necesitan solo unas pocas (entre 2 y 8) para que se forme un tumor. Sin embargo, tener estas mutaciones no es suficiente para que las células sean capaces de metastatizar. Para eso, las células necesitan adquirir varios programas que les ayuden a sobrevivir al estrés del proceso de metástasis.
Por eso, distintos tipos de tumores, aunque sean diferentes, desarrollan características similares que les permiten ser más propensos a la metástasis. Esto también brinda la oportunidad de crear tratamientos que se basen en biomarcadores, lo que significa que podrían ser efectivos para varios tipos de cáncer metastásico.
Aprovechando el sistema inmunológico para tratar la metástasis
Dado el impacto que tienen las terapias inmunológicas en tumores que antes se consideraban incurables, y teniendo en cuenta que el microambiente tumoral inmunológico (dónde por cierto, el ejercicio físico tiene su marco de acción) ha surgido como un factor clave en la regulación de la metástasis, revisamos en este documento estudios que se centran en la viabilidad y eficacia de la modulación inmune para tratar enfermedades metastásicas.
Bloqueo de los puntos de control inmunológico
Las terapias de bloqueo de puntos de control inmunológico, que se enfocan en proteínas como PD-1 y CTLA-4, son fundamentales para tratar muchos tipos de cáncer metastásico. Aunque algunas personas responden muy bien a estas terapias, muchos pacientes no tienen respuestas efectivas, y esto es un problema común.
Por ejemplo, en ciertos cánceres como el cáncer renal y el de hígado, estos tratamientos solo funcionan de manera moderada, mientras que en cánceres más resistentes, como los de mama y páncreas, los resultados son muy limitados. Sin embargo, combinar estos tratamientos con quimioterapia ha mostrado resultados prometedores. Además, hay una nueva generación de tratamientos en desarrollo que se dirigen a otros puntos de control inmunológico que podrían ayudar a mejorar la situación.
La segunda generación más notable de receptores de puntos de control inmunológico incluye TIM3, LAG3, TIGIT, B7-H3, Siglec-15 y VISTA, todos los cuales han mostrado potencial como objetivos antimetastáticos en diversas etapas de prueba clínica.
Habrá que estar pendientes, a nuevos ensayos clínicos.
Desarrollo de células inmunorreguladoras.
Los estudios han demostrado que en los tumores hay muchas células que ayudan al cáncer a crecer y a diseminarse. Para combatir el cáncer, es crucial eliminar ciertos tipos de células que tienen un papel supresor, como las células T reguladoras (Treg) y los macrófagos que están asociados con el tumor (TAM). Cuando se logran eliminar estas células, los tratamientos contra el cáncer tienden a funcionar mejor. Por ejemplo, algunos pacientes con melanoma han tenido mejores resultados cuando se combinan tratamientos que eliminan estas células con infusiones de otras células inmunológicas.
A pesar de su importancia, aún no hay muchos métodos efectivos para eliminar estas células en la práctica clínica. Las células Treg se forman a partir de otras células del sistema inmunológico y requieren señales específicas para madurar. Aunque se han intentado varios enfoques para deshacerse de ellas, muchos no han tenido éxito en pruebas clínicas.
Se han probado estrategias para modular los niveles de IL-2 y la abundancia del receptor CD25 en las células T, aunque los anticuerpos que eliminan CD25 también atacan las células T helper tipo 1 (TH1) y células NK, lo que causa una supresión inmune no deseada. A pesar de esto, terapias prometedoras como Synthorin IL-2 están siendo investigadas en múltiples tipos de tumores sólidos.
Perspectivas Futuras sobre el Tratamiento de la Enfermedad Metastásica
La metástasis del cáncer es un proceso complejo que depende de vías internas que fomentan la plasticidad y las respuestas al estrés, así como de vías externas que crean un entorno estromal inmunosupresor. Esto hace que el tratamiento de los cánceres metastásicos requiera estrategias terapéuticas más complejas en comparación con los enfoques centrados en los factores que causan los tumores primarios. Sin embargo, la evolución convergente de diferentes tipos de tumores durante la metástasis ofrece un gran potencial para tratamientos que no estén restringidos a un tipo específico de cáncer.
Algunos objetivos candidatos han sido validados como nodos clave de regulación y son compartidos entre diferentes tipos de cáncer. Por lo tanto, se debe adoptar una estrategia basada en biomarcadores para abordar los cánceres metastásicos, validando estrategias de un solo agente o combinaciones según la composición molecular de los tumores individuales. Los estudios recientes indican que eliminar factores inmunosupresores y dirigir tratamientos hacia las características intrínsecas del tumor serán enfoques centrales para mejorar la supervivencia general. Además, las terapias combinadas con mecanismos de acción distintos serán cruciales para prevenir la resistencia asociada a la metástasis y promover respuestas a largo plazo.
A pesar de esto, se ha prestado relativamente poca atención al descubrimiento de terapias que logren la regresión metastásica en modelos preclínicos. Aunque alcanzar este objetivo es uno de los mayores desafíos en la investigación, estas medidas deben convertirse en un indicador central de eficacia para guiar el desarrollo temprano de medicamentos. También se requerirá flexibilidad regulatoria para avanzar en estas nuevas clases de terapias de manera eficaz en términos de recursos.
Por ejemplo, se podrían utilizar marcadores farmacodinámicos predictivos como medidas secundarias clave, además de la supervivencia libre de progresión (PFS) y la supervivencia general (OS) a un año, especialmente en pacientes de alto riesgo. Esto es particularmente importante, ya que estos pacientes a menudo pasan por múltiples regímenes experimentales, lo que dificulta la evaluación de la OS.
Además, en la búsqueda de nuevos tratamientos, se debe priorizar la importancia de factores de estilo de vida y diagnóstico en la reducción de la mortalidad por cáncer, ya que una de las mayores amenazas a los recientes avances en este campo es el aumento de la incidencia del cáncer.
Espero que te haya parecido interesante!
Enhorabuena! Has completado la lectura de esta nueva entrega del blog.
Si est artículo ha cumplido con tus expectativas, te agradezco que me lo dejes reflejado en un me gusta.
Y si aún no estás suscrito al blog, hazlo para recibir este tipo de artículos todas las semanas de manera gratuita!